avec le soutien institutionnel du laboratoire Mayoly


Development and validation of AI-Assisted transcriptomic signatures to personalize adjuvant chemotherapy in patients with resectable pancreatic ductal adenocarcinoma
Auteurs : Nelson Dusetti, Nicolas Fraunhoffer, Pascal Hammel, Thierry Conroy, Rémy Nicolle, Jean-Baptiste Bachet, Alexandre Harlé, Vinciane Rebours, Anthony Turpin, Meher Ben Abdelghani, Emmanuel Mitry, James Biagi, Brice Chanez, Martin Bigonnet, Anthony Lopez, Ludovic Evesque, Thierry Lecomte, Eric Assenat, Olivier Bouché, Daniel Renouf, Aurélien Lamber, Laure Monard, Marjorie Mauduit, Jérome Cros, Juan Iovanna
Problématique : Le choix de la chimiothérapie adjuvante chez les patients atteints de cancer pancréatique repose principalement à ce jour sur des critères pronostiques. Des signatures transcriptomiques (ARN tumoral) assistées par IA ont été développées pour prédire l’efficacité de la gemcitabine, mais le FOLFIRINOX est devenu la chimiothérapie de référence en situation adjuvante.
But : Développer et valider des signatures transcriptomiques prédictives de l’efficacité de la gemcitabine et du FOLFIRINOX pour personnaliser la chimiothérapie adjuvante après résection d’un cancer pancréatique.
Matériels et méthodes : Signatures transcriptomiques assistées par intelligence artificielle développées à partir de lignées cellulaires (n>50), d’organoïdes (n>250) et de xénogreffes (n>150) puis validée et évaluée chez 349 patients inclus dans l’étude PRODIGE 24 (chimiothérapie adjuvante par FOLFIRINOX vs. Gemcitabine chez les patients opérés d’un cancer pancréatique).
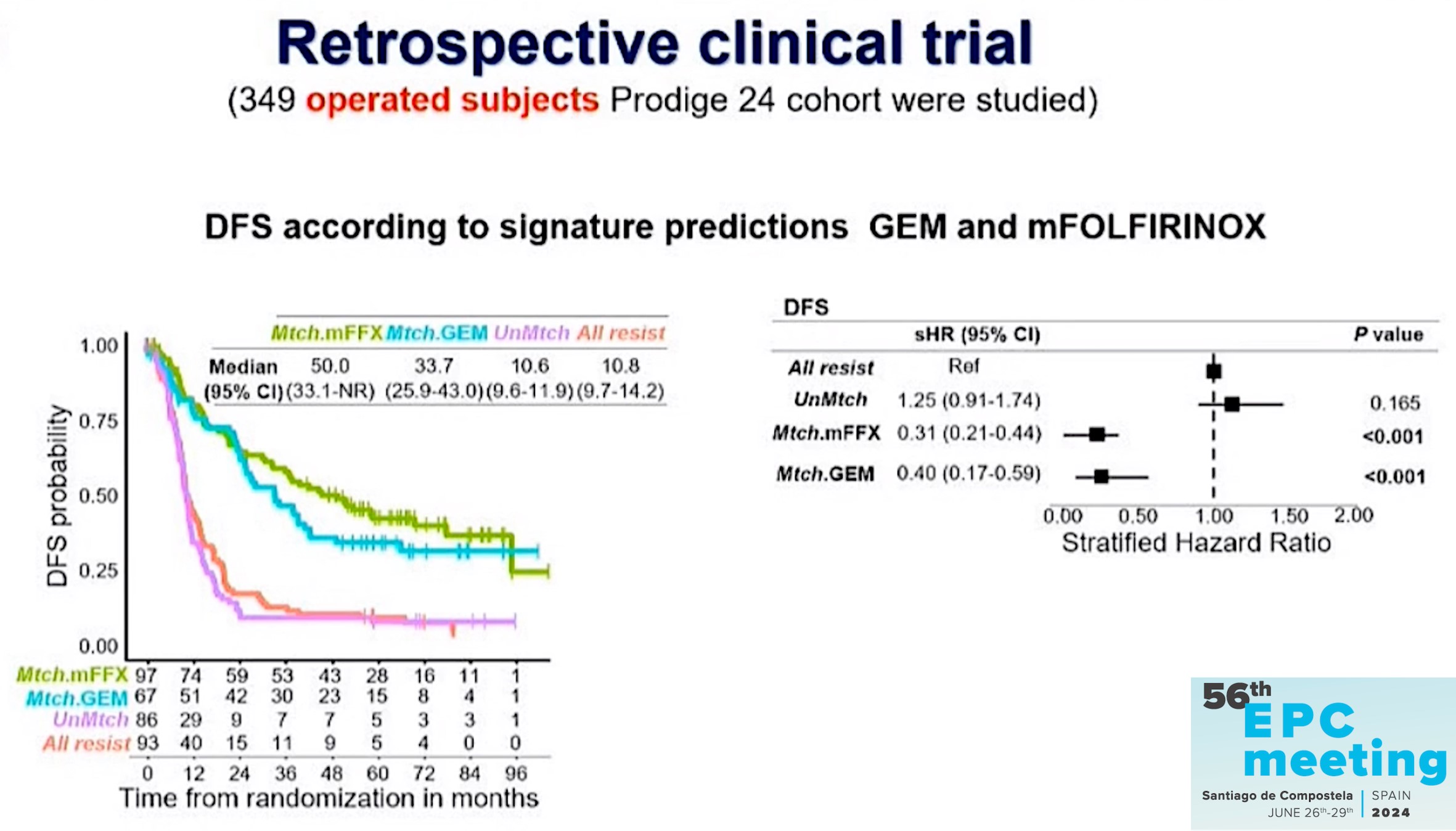
Résultats : L’efficacité de la chimiothérapie par FOLFIRINOX était corrélée au nombre de molécules (5FU, oxaliplatine, irinotécan) prédites comme sensibles. Les patients prédits comme sensible à 2-3 molécules étaient considérés comme sensibles au FOLFIRINOX (ffx+). Parmi les patients traités par FOLFIRINOX, ceux prédits sensibles au FOLFIRINOX (ffx+) avaient une meilleure SSR que ceux sans la signature (ffx-) : (50,0 vs. 13,9 mois ; HR 0,39 [0,26–0,57] ; p<0,001).
Parmi les patients traités par Gemcitabine, la signature ffx n’avait pas d’impact pronostique : la SSR était similaire entre ceux ayant une signature ffx+ et ceux ayant une signature ffx- (13,0 vs. 12,4 ; HR 0,86 [0,60–1,23] ; p=0,41).
De plus, les patients avec signature prédictive positive ffx+ ou Gem+ avaient une meilleure SSR quand ils recevaient la chimio correspondant à la signature (matched/ffx+ : 50,0 [33,1–NR] ; matched/gem+ : 33,7 [25,9–43,0]). A l’inverse, les patients traités par une chimiothérapie ne correspondant pas à leur signature avaient une mauvaise SSR (10,6 [9,6 – 11,9]), de même que les patients (27%) prédits comme résistants au FOLFIRINOX et à la gemcitabine (ffx-/gem-, 10,8 [9,7-14,2]).
Conclusions : L’administration d’une chimiothérapie adjuvante « adaptée » à la prédiction transcriptomique semble être associée à une efficacité supérieure de la chimiothérapie adjuvante (FOLFIRINOX ou gemcitabine).
Les patients prédits sensibles à gemcitabine et traités par gemcitabine semblent avoir une SSR similaire à ceux prédits sensibles au FOLFIRINOX et traités par FOLFIRINOX, au prix d’une moindre toxicité.
Ce travail pourrait également permettre d’identifier des des marqueurs et voie de signalisation des tumeurs prédites comme résistantes à tous les traitements.
Des études interventionnelles vont débuter prochainement pour confirmer prospectivement l’intérêt de la taylorisation de la chimiothérapie selon la signature transcriptomique, notamment en situation néodadjuvante (essai NEOPREDICT).
Intérêt pour le malade : 5/5
Applicabilité en pratique de routine : 3/5
Par Louis de Mestier