

3D genomic mapping reveals multifocality of human pancreatic precancers
[Nature 629, 679–687 (2024). https://doi.org/10.1038/s41586-024-07359-3]
Auteurs : A. Braxton, A. Kiemen, M. Grahn, A. Forjaz, J. Paarksong, J. Babu, J. Lai, L. Zheng, N. Niknafs, L. Jiang, H. Cheng, Q. Song, R. Reichel, S. Graham, A. Damanakis, C. Fischer, S. Mou, C. Metz, J. Granger, X. Liu, N. Bachmann, Y. Zhu, Y. Liu, C. Almagro-Pérez, A. Jiang, J. Yoo, B. Kim, S. Du, E. Foster, J. Hsu, P. Rivera, L. Chu, F. Liu, E. Fishman, A. Yuille, N. Roberts, E. Thompson, R. Scharpf, T. Cornish, Y. Jiao, R. Karchin, R. Hruban, P. Wu*, D. Wirtz* & L. Wood*.
Problématique justifiant la recherche ou l’étude : Les PanIN, lésions précancéreuses fréquentes à l’origine du carcinome canalaire pancréatique (PDAC), un cancer agressif au taux de survie à cinq ans de 11 %, restent mal comprises. Leur petite taille les rend invisibles à l’examen macroscopique, limitant les analyses à des coupes histologiques 2D incapables d’évaluer leur nombre, leur connectivité et leur architecture. Cette limite freine l’étude de leur évolution et de leur diversité génétique (KRAS, CDKN2A, TP53), encore incertaine : issues d’un clone unique ou indépendantes ? Pour mieux comprendre leur rôle dans la progression tumorale, il est crucial de coupler analyses tissulaires 3D et séquençage génétique.
But : Cette étude vise à cartographier en 3D les lésions PanIN humaines, en décrivant leurs topologies, leurs fréquences, leurs caractéristiques cellulaires et leurs altérations génétiques somatiques, afin d’évaluer leur multifocalité et de déterminer leur origine clonale. Pour cela, une reconstruction tissulaire 3D et une analyse génomique ciblée ont été combinées.
Materiel et méthodes : L’étude a porté sur des pancréas humains réséqués, exempts de cancer invasif, issus d’une cohorte de 46 échantillons macroscopiquement normaux, sectionnés en coupes de 5 μm (environ 1200 lames). Une coloration H&E toutes les 3 coupes a permis de reconstruire en 3D, à la résolution unicellulaire, à l’aide de CODA, un algorithme d’analyse d’image basé sur l’apprentissage automatique (Kiemen, Nature Methods 2022). Le nombre moyen de PanINs était de 13 par cm³ (jusqu’à 31). Plus de 889 lésions PanIN ont été identifiées manuellement, dont 37 ont été extraites par microdissection ciblée guidée par les reconstructions. Leur ADN a été analysé par séquençage ciblé (panel de 154 gènes) et WES pour cartographier les variations somatiques et évaluer les relations clonales et la distribution spatiale des lésions, à l’aide d’une microdissection laser des lésions sélectionnées.
Résultats : L’étude révèle que les PanINs sont omniprésents, multifocaux et largement indépendants sur le plan clonogénique. On extrapole que le pancréas humain contient en moyenne plus de 1 000 PanINs. La majorité (97 %) des PanINs séquencés possèdent des mutations KRAS, et 19 % contiennent plusieurs variants KRAS, suggérant une origine polyclonale. Le séquençage multi-régional et la détection in situ ont confirmé que ces mutations coexistent dans des sous-populations distinctes. De plus, la progression vers des lésions avancées (PanIN-3) et vers le PDAC s’accompagne de mutations supplémentaires dans TP53 ou SMAD4, absentes dans les PanINs de bas grade
Etonnamment des lésions très proches anatomiquement pouvaient être génétiquement non apparentées, tandis que des foyers éloignés dans l’organe partageaient parfois des mutations communes. La reconstruction phylogénétique a confirmé que chaque pancréas possédait une mosaïque complexe de clones précancéreux distincts. La cartographie 3D est donc essentielle à l’étude des prémices du cancer pancréatique
Conclusion : Cette étude démontre que les lésions précancéreuses du pancréas ne sont pas nécessairement liées entre elles. Leur survenue semble être un phénomène multifocal et stochastique, ce qui remet en question l’idée d’une progression tumorale linéaire à partir d’un clone fondateur unique. La majorité (97 %) des PanINs séquencés possèdent des mutations KRAS, et 19 % contiennent plusieurs variants KRAS, suggérant une origine polyclonale. La combinaison d’une reconstruction 3D de haute résolution avec une cartographie génétique ciblée offre une vision entièrement nouvelle de la pré-carcinogenèse pancréatique et ouvre la voie à des approches plus fines pour la détection et la surveillance des lésions à risque. Ces résultats ouvrent la voie à la détection précoce ciblée des PanINs à risque et à la modélisation 3D de lésions précancéreuses en y incorporant des données de protéomiques et de transcriptomiques spatiales, comme l’explore la prochaine étude des auteurs, actuellement en pre-print doi.org/10.1101/2025.06.08.658506.
Intérêt pour le malade : 4/5
Applicabilité en pratique de routine : 3/5
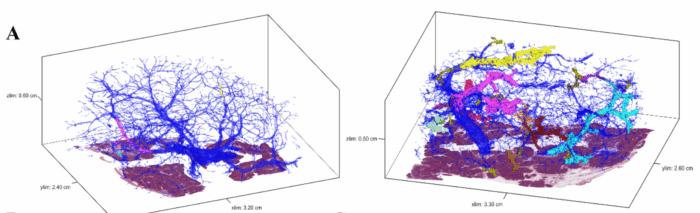
Figure 1 : Modèles 3D représentatifs de deux blocs de tissu pancréatique humain.
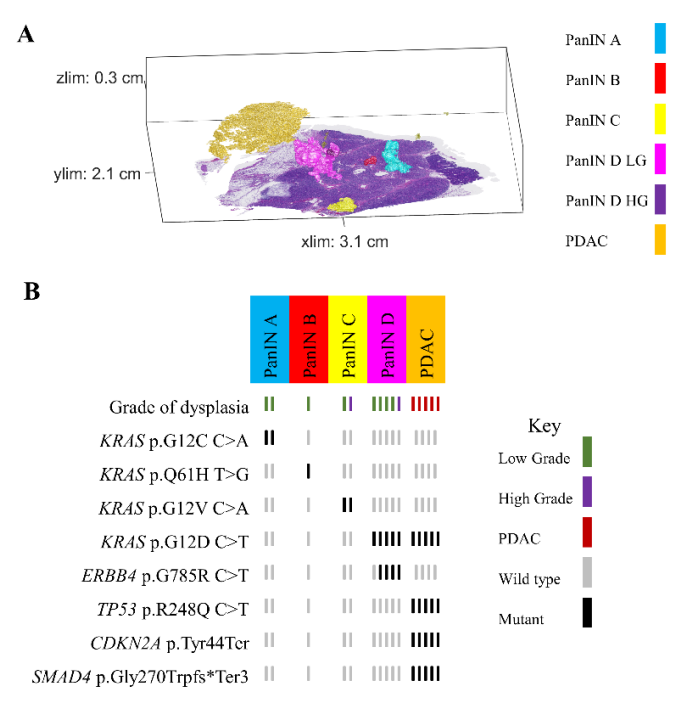
Figure 2 : Modèle 3D d’un tissu pancréatique grossièrement normal montrant de multiples PanINs spatialement distinctes, chacune représentée par des couleurs uniques (A). Tableau des mutations avec les résultats du séquençage ciblé, où chaque colonne correspond à une lésion spatialement distincte, et dont les couleurs des lésions correspondant au modèle 3D (B).
Par Sébastien Frey et Yvan Martineau

