

Integration of AI model into ampulla of Vater : Challenges and solutions
Auteurs : Seong Ji Choi, Séoul, Corée du Sud
Problématique justifiant la recherche ou l’étude : Au cours des dernières années, plusieurs études ont mis en évidence une reconnaissance efficace des polypes colorectaux au cours d’une coloscopie, et la prédiction de leur malignité, par un modèle d’intelligence artificielle (IA). A l’inverse, et malgré ces progrès de l’IA, peu d’outils ont été développés pour aider en temps réel l’endoscopiste lors de la CPRE. Pourtant, la reconnaissance d’une lésion ampullaire et la prédiction de sa malignité pourraient être des outils d’assistance intéressant. Les variations anatomiques de l’ampoule de Vater compliquent sa détection, surtout chez les endoscopistes peu expérimentés, entraînant un risque accru d’échecs et de complications. Nous présentons ici deux travaux réalisés par l’auteur.
But : Développer un algorithme d’apprentissage profond (deep learning) capable de :
- Détecter automatiquement la localisation de l’ampoule de Vater (1ère étude).
- Prédire la difficulté de la cannulation sélective vers le canal biliaire principal (1ère étude)
- Classer une ampoule normale vs pathologique (dysplasie vs cancer) (2ème étude, non publiée).
Matériel et méthodes : A partir de données rétrospectives multicentriques, en Corée du Sud, une base d’images de CPRE a été construite.
Dans la première étude, une annotation indiquant la localisation de l’ampoule de Vater a été effectué sur un total de 451 images. Le modèle utilisé était le réseau de neurone U-Net. Pour la classification de la difficulté de cannulation, les images ont été classées en cas faciles ou difficiles (binaire), et selon 4 niveaux (facile, temps > 5 min, techniques additionnelles, échec).
Dans la deuxième étude, une classification a été réalisé, selon les données histologiques, avec ‘papille non pathologique’ (n=483), ‘papille dysplasique’ (n=261), et papille adénocarcinomateuse’ (n=285). La base d’entraînement de l’algorithme a été augmentée grâce à un un type de réseau de neurones capable de générer des images réalistes, le réseau adversarial génératif, ou GAN (Generative Adversarial Network). Le développement de l’algorithme a été réalisé par une plateforme d’apprentissage profond automatisé, Neuro-T®.
Résultats : La précision de la reconnaissance de l’ampoule de Vater était de 76.2%. La distance du centroïde, e.g. la mesure d’erreur entre le centre de la « vraie » position de l’ampoule et celle prédite, était de 0.021 (plus elle proche de 0 et plus elle est précise). La prédiction de la difficulté de cathétérisme avec une précision maximale de 71.2%. La focalisation du modèle, évaluée par une fonction Grad-CAM, démontre que son attention se porte sur des zones anatomiques pertinentes.
Quant à la précision de la prédiction histologique de la papille, elle était de 93.1% pour les papilles non pathologiques, de 88.9% pour les papilles dysplasiques, et de 91.9% pour les papilles adénocarcinomateuses.
Conclusion : Le modèle IA développé est capable d’identifier précisément l’ampoule de Vater et d’estimer la difficulté de la cannulation pendant l’ERCP, avec des performances intéressantes. De manière plus intéressante, les capacités de l’IA à déterminer l’histologie d’une lésion papillaire sont très élevées. Ces premiers résultats sont prometteurs pour le développement d’outils d’IA, et pourraient améliorer la qualité et la sécurité des procédures, en particulier pour les praticiens moins expérimentés.
Intérêt pour le malade : 3/5. Amélioration potentielle du diagnostic et de la sécurité, mais encore à l’état expérimental.
Applicabilité en pratique de routine : 3/5. Prometteur, mais nécessite validation prospective et intégration technique.
Références :
Kim T, et al. Artificial intelligence-assisted analysis of endoscopic retrograde cholangiopancreatography image for identifying ampulla and difficulty of selective cannulation. Sci Rep. 2021 Apr 16;11(1):8381. doi: 10.1038/s41598-021-87737-3.
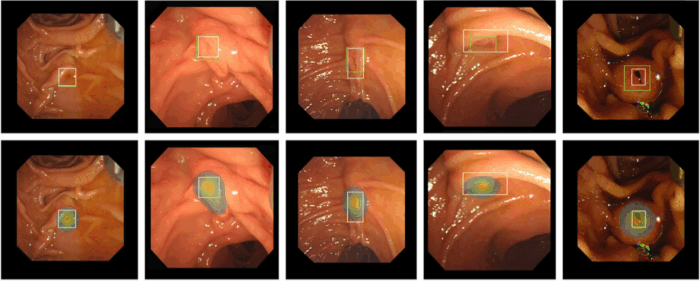
Figure 1 : Reconnaissance de l’ampoule de Vater (boîte de délimitation) et de l’attention portée par l’algorithme (carte de densité, fonction Grad-CAM)

Figure 2 : Résultats du modèle dans la prédiction histologique de l’ampoule.
Par Sébastien Frey
